Nejdříve si vyjasněme pojmy: držíme-li v ruce železnou tyč, mluvíme někdy o železe, někdy o oceli - v obou případech se v praxi jedná o slitinu železa s uhlíkem (neuvažuji o chemicky čistém železe pro laboratorní účely), budu tedy používat pojem ocel pro železo s obsahem uhlíku do 2 %. (při vyšším obsahu se jedná o litinu). Přítomnost uhlíku v hutnicky vyráběném železe vyplývá z technologického procesu , kdy se železo získává redukcí oxidů železa (železná ruda) uhlíkem (koks) ve vysoké peci.
Obsah uhlíku (C) v železe (Fe) je klíčovým faktorem pro vlastnosti oceli a je dán následným zpracováním surového železa. Uhlík se v železe (v malých koncentracích) poměrně snadno rozpouští a tvoří se sloučeniny (karbidy železa), nebo tuhý roztok uhlíku v železe. Vlastnosti oceli určuje právě forma, v jaké se uhlík v oceli vyskytuje.
Zjednodušeně řečeno za různých podmínek (kombinace různé teploty a obsahu uhlíku) můžeme v tuhé fázi nalézt :
tuhý roztok
uhlíku v železe δ
(delta) - pro nás naprosto nezajímavý, vyskytuje se jen do 0,02% C
tuhý roztok uhlíku v železe γ (gama) - austenit - pro nás významná krystalová struktura, neboť její vznik je nezbytný při kalení
martenzit - jeho vznik je podstatou kalení - je to krystalová struktura, která vzniká rozpadem austenitu při rychlém ochlazování
bainit a perlit - další krystalové struktury vznikající při tepelném zpracování oceli
karbid železa Fe3C - cementit
volný uhlík C - grafit
železo α - nejčastěji se vyskytující krystalová struktura v oceli za normální teploty
(Neděste se, nejsme ve škole, nikdo vás
zkoušet nebude. Bez toho se ale to co probíhá při kalení nedá vysvětlit.)tuhý roztok uhlíku v železe γ (gama) - austenit - pro nás významná krystalová struktura, neboť její vznik je nezbytný při kalení
martenzit - jeho vznik je podstatou kalení - je to krystalová struktura, která vzniká rozpadem austenitu při rychlém ochlazování
bainit a perlit - další krystalové struktury vznikající při tepelném zpracování oceli
karbid železa Fe3C - cementit
volný uhlík C - grafit
železo α - nejčastěji se vyskytující krystalová struktura v oceli za normální teploty
Na obrázku vidíte rovnovážný diagram soustavy Fe - C. Slovo rovnovážný tady znamená, že za daných teplot a složení je soustava stabilní, to je, že jiné sloučeniny ani krystalové struktury nevznikají - jinými slovy není to stav vzniklý náhlým ochlazením, nebo ohřátím. Pro kováře je důležitých několik čar na diagramu. Předně jsou to čáry ohraničující shora tuhou fázi - nad touto teplotou je kov tekutý, nebo je tvořen směsí taveniny a pevných částic ( na této teplotě se budeme pohybovat možná při svařování v ohni, ale jinak ne). Dále jsou to hranice oblasti existence austenitu a nakonec teplota 727°C - mez přeměny železa α na železo γ (gama). To je minimální teplota, nad kterou se musí ocel ohřát, aby kalení mělo vůbec nějaký smysl.
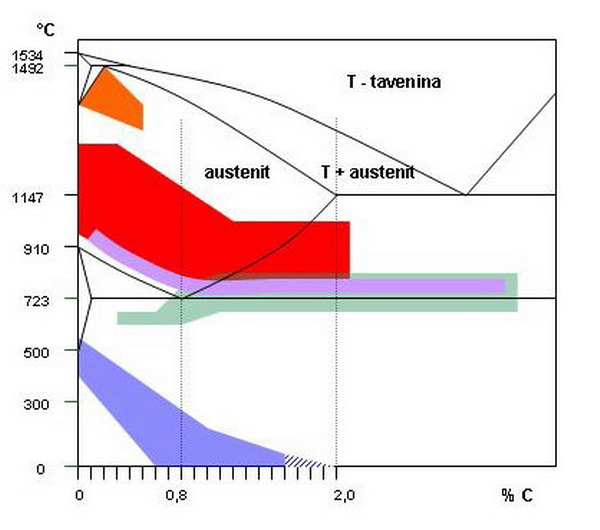
Dále je v grafu několik barevně vyznačených oblastí:
červená - oblast
kovacích teplot
oranžová - oblast teplot pro kovářské svařování
zelená - oblast žíhání na měkko
fialová-- oblast kalicích teplot
modrá -- oblast tvorby martenzitu
oranžová - oblast teplot pro kovářské svařování
zelená - oblast žíhání na měkko
fialová-- oblast kalicích teplot
modrá -- oblast tvorby martenzitu
Procesy probíhající při kalení
Konečně jsem se prokousal přes teorii k vlastnímu procesu kalení, kvůli kterému jsem psal tento článek.
Předně je potřeba říci, že průběh kalicích procesů závisí na složení oceli a tedy nelze jednoduše popsat nějaký univerzální postup. Kromě obsahu uhlíku má na kalicí proces zásadní vliv přítomnost legujících prvků (chrom, vanad, molybden, wolfram), které se přidávají do oceli právě za účelem zvýšení tvrdosti, pevnosti...
1. Ohřev na kalicí teplotu
Kalicí teplota je volena podle obsahu uhlíku tak aby došlo ke vzniku austenitické struktury, ale současně nezhrublo zbytečně zrno
(zájemce o podrobnosti odkazuji na knihu
Strojírenské materiály, Pluhař, Koritta, SNTL 1981, ze které jsem čerpal).
Na obrázku je vyznačena fialově. Podmínkou je aby ohřev probíhal v
redukčním prostředí, kde nedojde k oduhličení povrchu. Vzniklý
austenit není magnetický - tedy magnet uvázaný na kusu drátu se k
němu NEPŘITÁHNE. (u ocelí s vysokým obsahem uhlíku a legujících prvků
jsem to nezkoušel)
2. Výdrž na
kalicí teplotěVýdrž by měla
být několik minut, ne zbytečně dlouho - (víc se mi opravdu zjistit
nepovedlo). teplota by měla být opravdu jen ta, která je v grafu,
vysoká teplota je na škodu. Opět připomínám, že v ohni s přebytkem
vzduchu může dojít k oduhličení (vypálení uhlíku), tedy ocel ztratí to
co ji dělá uhlíkatou ocelí. Ohřev v peci, resp. plynové výhni dovoluje
samozřejmě přesnější určení teploty
3.
OchlazováníAž
potud to byla celkem jednoduchá záležitost. Učené knihy říkají, že pro
dosažení nejvyšší tvrdosti (nejvyššího obsahu martenziu) se dosáhne
ochlazováním takzvanou nadkritickou rychlostí. Martenzit vzniká jen při
ochlazování - pokud teplota materiálu klesá - jakmile se teplota
zastaví, zastaví se i vznik martenzitu (vznik martenzitu je
prostě určité přeskupení atomů uvnitř krystalové mřížky). Rozmezí teplot, při kterých martenzit
při ochlazování (pozor jen při
ochlazování - zpátky ohřevem to nejde) vzniká je vyznačena modře. (podrobnější údaje pro
jednotlivé oceli se mi zatím získat nepovedlo).
Jak a čím dosáhnout chlazení nadkritickou rychlostí bude zřejmě docela věda. Ono totiž příliš rychlé ochlazování přináší i velké nebezpečí deformací a prasklin v materiálu, někdy mikroskopických jindy dobře viditelných (moje vlastní zkušenost, kterou jsem získal po několikahodinové výrobě útinky, která praskla po celé délce při kalení do vody).
Voda - je dobře k mání, není problém jí mít velké množství. Chlazení je ale nerovnoměrné, nehodí se pro vysoce uhlíkaté a legované oceli.
Kalicí lázně - koncentrované vodné roztoky některých sloučenin - chrání povrch před oduhličením během chlazení, regulují odvod tepla - do této oblasti jsem zatím nepronikl, takže neporadím ani jak ani proč
Olej - rovnoměrnější, pomalejší chlazení,. Musí ho být hodně (30 - 50 litrů), jinak se rychle ohřeje a kalení se zastaví
!!!! POZOR OLEJ HOŘÍ !!!!
Solné taveniny - mimo možnosti kovárny.
Jak a čím dosáhnout chlazení nadkritickou rychlostí bude zřejmě docela věda. Ono totiž příliš rychlé ochlazování přináší i velké nebezpečí deformací a prasklin v materiálu, někdy mikroskopických jindy dobře viditelných (moje vlastní zkušenost, kterou jsem získal po několikahodinové výrobě útinky, která praskla po celé délce při kalení do vody).
Voda - je dobře k mání, není problém jí mít velké množství. Chlazení je ale nerovnoměrné, nehodí se pro vysoce uhlíkaté a legované oceli.
Kalicí lázně - koncentrované vodné roztoky některých sloučenin - chrání povrch před oduhličením během chlazení, regulují odvod tepla - do této oblasti jsem zatím nepronikl, takže neporadím ani jak ani proč
Olej - rovnoměrnější, pomalejší chlazení,. Musí ho být hodně (30 - 50 litrů), jinak se rychle ohřeje a kalení se zastaví
!!!! POZOR OLEJ HOŘÍ !!!!
Solné taveniny - mimo možnosti kovárny.
4.
Popouštění
Martenzit
je tvrdý, ale křehký.
Popouštěním se dá dosáhnout určitých změn ve struktuře kovu, při
kterých vznikají houževnatější produkty (příšerná věta
- část martenzitu se rozpadne a vzniklé produkty sice nejsou tak tvrdé,
ale ani tak křehké). druhým důvodem pro popouštění je odstranění
vnitřního pnutí.
Popouštění je ohřátí na nízkou teplotu, při které se martenzit částečně rozpadá. Dá se provést jednak po úplném ochlazení, opětovným opatrným ohřátím (v oleji, na kovové desce ohřívané zespodu, v peci), nebo tak, že se využije vnitřního tepla. To znamená, kov se rychle povrchově ochladí, pak se vyndá a nechá se ohřát zbytkovým teplem zevnitř (napouštění). (no a tohle je právě ta praxe, na kterou je teorie krátká - rád tu dám prostor zkušeným).
Popouštěcí teplota opět závisí na druhu oceli a na účelu popouštění. Základní popouštění je u uhlíkových ocelí na teplotu do 350°C Popouštění pérových ocelí se provádí v rozmezí teplot 350 - 450°C, některé konstrukční oceli se popouští až na 700°C. Doba popouštění (výdrže na teplotě) je 30 min až 10 hodin ( toho asi v kovárně těžko dosáhneme).
Nejjednodušším způsobem použitelným v kovárně je již zmíněné napouštění - ohřev vnitřním teplem na teplotu 220 - 300°C. Po rychlém povrchovém ochlazení (zamočení do vody) pilníkem, nebo bruskou rychle obrousíme malou plošku, aby bylo možno pozorovat povrch kovu. Ke stanovení dosažené teploty využijeme takzvané nabíhání čerstvě obroušeného povrchu. Na povrchu se vytváří tenká vrstva oxidů, která je podle teploty různě barevná. Uvedeným teplotám tedy odpovídá slámově žlutá až modrá barva. Barvy najdete na stránce Tabulky teplot. Po popuštění se materiál úplně ochladí.
Popouštění je ohřátí na nízkou teplotu, při které se martenzit částečně rozpadá. Dá se provést jednak po úplném ochlazení, opětovným opatrným ohřátím (v oleji, na kovové desce ohřívané zespodu, v peci), nebo tak, že se využije vnitřního tepla. To znamená, kov se rychle povrchově ochladí, pak se vyndá a nechá se ohřát zbytkovým teplem zevnitř (napouštění). (no a tohle je právě ta praxe, na kterou je teorie krátká - rád tu dám prostor zkušeným).
Popouštěcí teplota opět závisí na druhu oceli a na účelu popouštění. Základní popouštění je u uhlíkových ocelí na teplotu do 350°C Popouštění pérových ocelí se provádí v rozmezí teplot 350 - 450°C, některé konstrukční oceli se popouští až na 700°C. Doba popouštění (výdrže na teplotě) je 30 min až 10 hodin ( toho asi v kovárně těžko dosáhneme).
Nejjednodušším způsobem použitelným v kovárně je již zmíněné napouštění - ohřev vnitřním teplem na teplotu 220 - 300°C. Po rychlém povrchovém ochlazení (zamočení do vody) pilníkem, nebo bruskou rychle obrousíme malou plošku, aby bylo možno pozorovat povrch kovu. Ke stanovení dosažené teploty využijeme takzvané nabíhání čerstvě obroušeného povrchu. Na povrchu se vytváří tenká vrstva oxidů, která je podle teploty různě barevná. Uvedeným teplotám tedy odpovídá slámově žlutá až modrá barva. Barvy najdete na stránce Tabulky teplot. Po popuštění se materiál úplně ochladí.